2026年2月6日
Hims株価急落 FDA警告受け

先週末(2026年2月6日)、Hims & Hers Healthの株価が急落しました。きっかけは同社が今月発表した「月額49ドル」という破格の肥満予防薬。これが規制当局や製薬大手の強い反発を招く結果となり、株価下落につながりました。なぜ期待の新商品がリスクと見なされたのか、最新の報道をもとに、その背景をわかりやすく解説します。
(本記事は、公開情報に基づく分析および筆者の見解を示したものであり、その正確性や完全性を保証するものではありません。株価や企業の将来を保証せず、また特定の政治的立場や政策を支持・推奨する意図も一切ありません。投資判断や経済的判断は、ご自身の責任で行ってください。)「月額49ドル」の衝撃と踏み越えた一線
今回の株価下落の引き金となったのは、同社が2月5日(米国時間)に打ち出した大胆な価格戦略でした。同社は、高額な減量薬「ウゴービ」と同じ成分だとする飲み薬を、調剤という仕組みで作り、初月49ドルで提供すると発表しました。
この破格の値段での肥満薬提供は、競合のノボノルディスクとイーライリリーに衝撃を与え、両者の株価を一時下げる形となっていました。

ノボノルディスクはこのHimsの安価な飲み薬販売に強く反発しました。未承認の調剤品が、承認薬の代替のように広く売り込まれることは、制度の趣旨や患者の安全性の観点から問題だとして、法的・規制上の対応も辞さない構えを示しました。
FDAは警告 「規制のために材料を制限する」
6日、米食品医薬品局(FDA)は「承認されていない調剤のGLP-1薬が、承認薬に似た代替品として大量に宣伝・販売されている状況を問題視している」と名指しで警告。
GLP-1とは、食欲や血糖の調整に関わる体内ホルモンの名前で、減量薬ではこの働きを利用して「食欲を抑えやすくする」「血糖を下げる方向に働く」とされる薬が使われます。一般にはまとめて「GLP-1薬」と呼ばれています
FDAが注意喚起で終わらせず、具体策まで言い切りました。FDAは、そうした非承認の調剤GLP-1に使われる有効成分の原材料について、「制限するための断固とした措置を取る」と表明しています。
つまり、出来上がった薬を注意するだけでなく、「そもそも作るための材料の流れを締める」という宣言です。材料が絞られれば、供給停止やコスト上昇などにより、ビジネスが続けたくても続けられない方向に振れます。
さらにFDAは、非承認の調剤品を「承認薬と同等」「後発医薬品(ジェネリック)」と受け取られる形で売り込むことや、根拠の薄い健康効果をうたうことに対して、手段を用いて対応するとしています。
FDAの姿勢は強く、必要なら警告書簡だけでなく、押収や差し止めといった法的措置もあり得る、という姿勢も示しています。
こうした警告が出たことで、このやり方で稼ぐ筋道そのものが塞がれるのではないかという点が懸念されました。
以上のようなFDAの強硬姿勢が伝わった局面で株価が時間外で大きく下落する結果となりました。
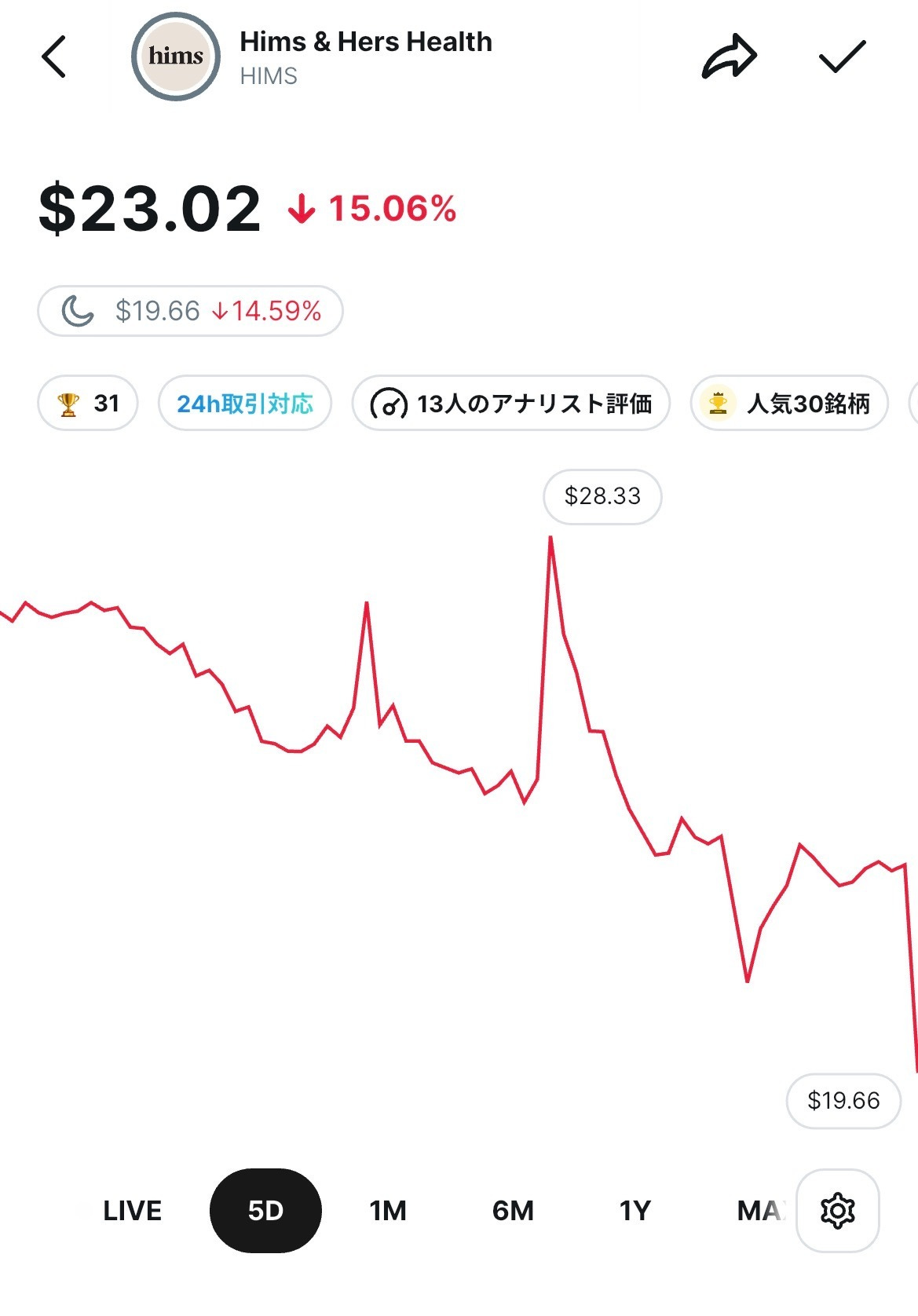
Hims & Hers Health の過去5日間の株価 / Woodstock
発売開始2日で販売停止
そして、Himsは当該飲み薬の発売開始二日後、販売中止を発表しました。ブルームバーグによると同社は、業界関係者との協議を踏まえ、X(旧ツイッター)で「提供を中止する」と説明。提供開始からわずか2日ほどでの撤回は、株価の重しになりました。
医療を所管する当局がこの件を司法当局に回したと報じられ、捜査や法的措置につながる可能性が意識されるようになりました。報道によれば、米保健福祉省の法律顧問が「連邦食品・医薬品・化粧品法に違反した疑い」を司法省に伝えたとXで明らかにしたとされています。
FDAの発表を受けて時間外取引で同社株が約13%下落した一方、大手製薬企業ノボ・ノルディスクの米国預託証券は一時上昇。規制強化が「模倣品側の逆風」「正規品側の追い風」と受け止められた構図も浮かびます。ノボ側は「未承認の模倣薬や非正規の有効成分が患者にもたらしかねないリスク」を理由に、当局の措置を歓迎したとも報じられています。
今後の焦点
今後の焦点は、二つです。
一つは、GLP-1薬をどういう形で提供するのかを、当局の線引きに沿って作り直せるかどうかです。FDAは「未承認の調剤GLP-1を、承認薬の代替のように大量に売り込む動き」に強い姿勢を示しました。ここに正面から答えない限り、不透明感は残りやすいでしょう。
二つ目は、減量薬が止まっても会社が成長できる形に変われるかです。今回の件で市場が不安になったのは、「減量薬が規制で止まると、成長ストーリーそのものが崩れかねない」と見えたからです。市場が見ているのは、減量薬以外でも売上を作れるのか、そして減量薬についても当局の線引きに沿う形へ切り替えられるのか、という点です。
報道によれば同社は「法令順守」を強調し、手頃な医療への安全なアクセス確保のため当局と協議を続ける考えも示したとされます。
製薬市場の対立や当局の追加対応が注目されます。
参考文献
本記事は、2026年2月9日時点の以下の情報を基に構成しています。
- Madison Muller, Jessica Nix(2026年)「米FDA、肥満症治療薬の模倣品規制へ-ヒムズ&ハーズなどが販売」『ブルームバーグ』2026年2月6日(更新:2026年2月7日), https://www.bloomberg.com/jp/news/articles/2026-02-06/TA256MT96OSJ00 (参照日:2026年2月9日).
- Leah Douglas, Siddhi Mahatole(2026年)“US signals crackdown on compounded weight-loss drugs; Hims shares tumble”『ロイター』2026年2月6日(更新:2026年2月7日), https://www.reuters.com/business/healthcare-pharmaceuticals/fda-restrict-glp1-ingredients-used-nonapproved-compounded-drugs-2026-02-06/ (参照日:2026年2月9日).
- Anushadevan Shah, Amina Niasse(2026年)“Hims to stop offering GLP-1 pill after FDA warned of crackdown”『ロイター』2026年2月7日, https://www.reuters.com/legal/litigation/hims-hers-stop-offering-compounded-semaglutide-pill-after-fda-crackdown-2026-02-07/ (参照日:2026年2月9日).
- Carlos Méndez, Chris Thomas(2026年)“Hims shares plunge after FDA threatens action on ‘illegal copycat drugs’”『ロイター』2026年2月5日(更新:2026年2月6日), https://www.reuters.com/legal/litigation/fda-take-action-companies-marketing-illegal-copycat-drugs-fda-chief-says-2026-02-05/ (参照日:2026年2月9日).
- 米食品医薬品局(FDA)(2026年)“FDA Intends to Take Action Against Non-FDA-Approved GLP-1 Drugs” Press Announcement, 2026年2月6日,https://www.fda.gov/news-events/press-announcements/fda-intends-take-action-against-non-fda-approved-glp-1-drugs (参照日:2026年2月9日).
Woodstock | ウッドストック 手数料完全無料・24時間取引アプリ
弊社Woodstock(ウッドストック)では、米国株式投資アプリを運営しています。
Woodstockアプリでは、
- 手数料完全無料(為替手数料・出金手数料・取引手数料・残高手数料)
- 24時間取引
- 200円から投資可能
など投資のハードルを下げ、投資をもっと自由にするサービスを提供しています。
手数料無料でいつでも取引できるというシームレスな体験をぜひご体験ください。
アプリダウンロードはこちらのリンクか画像をタップより。